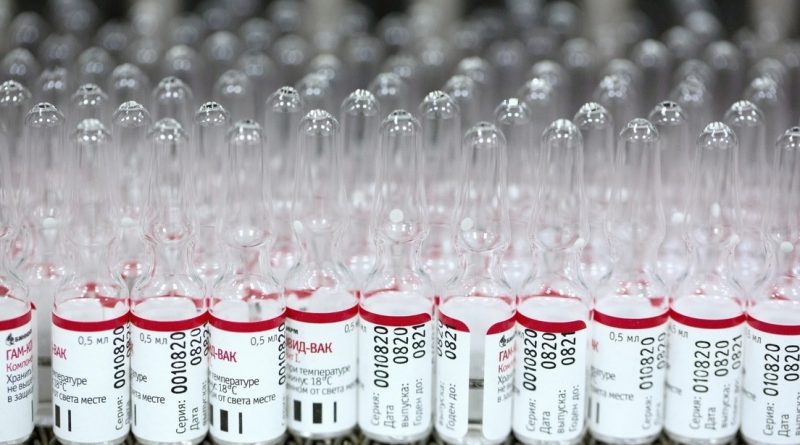
La farmacéutica Uniao Química acuerda con Rusia el suministro de 10 millones de dosis de Sputnik V a Brasil en el primer trimestre de 2021
Por RT Internacional
Esta semana, la compañía brasileña junto con el Fondo Ruso de Inversión Directa (RDIF) solicitarán la autorización del uso de emergencia.
La farmacéutica Uniao Química acordó con el Fondo Ruso de Inversión Directa (RDIF) el suministro de 10 millones de dosis de la vacuna Sputnik V a Brasil en el primer trimestre de 2021, con entregas desde este mismo mes de enero.
El acuerdo fue alcanzado durante una reunión entre el director general del RDIF, Kirill Dmitriev, y el presidente de Uniao Química, Fernando De Castro Marques. Tras el encuentro, se informó que ambas entidades solicitarán esta semana la autorización del uso de emergencia de Sputnik V a la Agencia Nacional de Vigilancia Sanitaria (Anvisa) de Brasil.

Como parte de la asociación entre estas dos organizaciones, RDIF, además, ha facilitado la transferencia de tecnología para la producción de la vacuna rusa en Brasil, que ya comenzó este mes de enero.
“Nuestros socios de Uniao Química estuvieron entre los primeros en el mundo en mostrar interés en la vacuna rusa Sputnik V. Por nuestra parte, estamos listos para una cooperación a gran escala en suministros y producción para comenzar la vacunación de la población en Brasil lo antes posible”, dijo Dmitriev.
De momento, la vacunación comenzó con los brasileños que trabajan en la Embajada del país sudamericano en Rusia.
Dmitriev añadió que el RDIF y Uniao Química esperan suministrar150 millones de dosis a Brasil en este año. Además, enfatizó que “Sputnik V es una vacuna segura y eficaz, creada sobre una plataforma probada y bien investigada de vectores adenovirales humanos”.
Esta vacuna rusa ya recibió la autorización de uso de emergencia en varios países, como Argentina —donde ya comenzó la vacunación—, Bolivia, Argelia, Serbia y Palestina.
Pendiente en ANVISA
La farmacéutica Uniao Química solicitó a Anvisa la autorización para iniciar la fase 3 de las pruebas de Sputnik V en Brasil, uno de los requisitos que ha pedido la propia agencia para aprobar el uso de emergencia.
No obstante, hasta ahora Anvisa no ha dado respuesta a esa solicitud, que fue presentada a finales de diciembre.